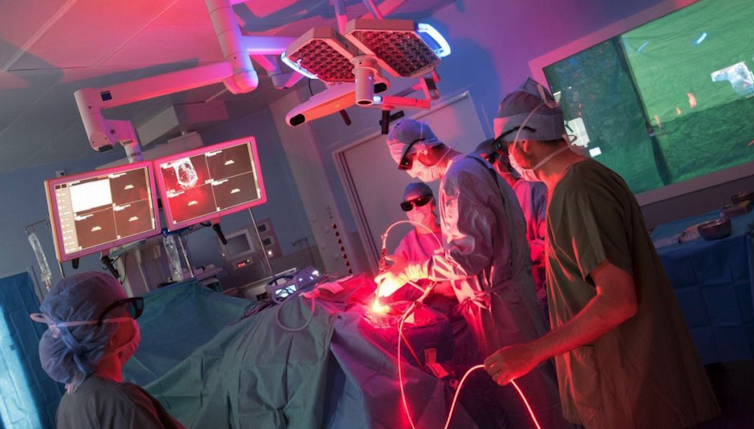
Inserm Oncothai Lille, CC BY
Céline Frochot, Université de Lorraine et Serge Mordon, Institut national de la santé et de la recherche médicale (Inserm)

Nous vous proposons cet article en partenariat avec l’émission de vulgarisation scientifique quotidienne « La Tête au carré », présentée et produite par Mathieu Vidard sur France Inter. L’auteur de ce texte évoquera ses recherches dans l’émission du 26 octobre 2018 en compagnie d’Aline Richard Zivohlava, éditrice sciences et technologie pour The Conversation France.
On l’appelle la thérapie photodynamique. En 2016, nous évoquions dans The Conversation cette technique peu connue du grand public et pourtant utilisée cliniquement pour certains types de cancers : une molécule photoactivable est déposée sur une lésion, et activée avec de la lumière afin de détruire localement les tissus touchés. Les dermatologues, notamment, utilisent quotidiennement la PDT pour traiter des lésions pré cancéreuses de la peau.
Aujourd’hui, la technologie s’affine. Pour illuminer de façon homogène une zone entière, par exemple la tête, un textile lumineux a été conçu à Lille. Il est fait de fibres optiques tricotées, une innovation de la société Texinov, financée par l’Europe. Les résultats d’une évaluation sur plusieurs centres hospitaliers montrent que 95 % des lésions sont détruites, sans aucune douleur. En effet, ce dispositif innovant est utilisé avec une irradiance faible (de l’ordre de 2 mW/cm2) et pendant une durée de 2 heures.

Auteurs, CC BY
Les avancées ne concernent pas seulement la dermatologie. En urologie, la société Steba-biotech a développé un nouveau photosensibilisateur, la padeliporfin, pour le traitement du cancer de la prostate. Ce traitement est autorisé dans plusieurs pays d’Amérique centrale et du sud depuis fin 2015. En Europe, après un essai clinique réalisé sur 413 patients dans 47 sites hospitaliers, cette procédure a été autorisée en novembre 2017. Entre le 8 mars 2011 et le 30 avril 2013, 206 patients ont eu un traitement PDT et 207 patients une surveillance active. Après deux ans, moins d’un tiers du groupe PDT a vu sa maladie progresser, contre plus d’un sur deux dans le groupe témoin. Près d’un patient sur deux au sein du groupe PDT présentait un résultat négatif à la biopsie de la prostate, indiquant une rémission complète, contre moins de un sur six dans le groupe témoin.
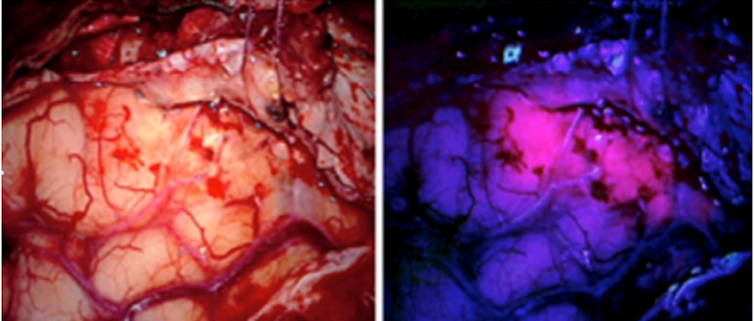
Tumeur colorisée en rose
Pour le traitement du glioblastome, cancer du cerveau au pronostic très sombre, un essai clinique a été mis en place en mai 2017 à Lille. A ce jour 9 patients ont été traités par thérapie photodynamique. La technique consiste à faire boire au patient, 5 heures avant l’intervention chirurgicale, une substance qui va permettre de guider le neurochirurgien lors de la résection de la tumeur. En effet, cette substance est spécifiquement accumulée dans les cellules tumorales. Au bloc chirurgical, le chirurgien utilise son microscope avec une lumière bleue afin de mieux voir la tumeur qui apparaît en rose. Un ballonnet, développé par l’unité Oncothai, est ensuite introduit dans la cavité obtenue après chirurgie. Une illumination en lumière rouge permet alors de détruire alors les cellules tumorales résiduelles situées en périphérie de la cavité. Il faut souligner que c’est la première fois que la PDT est proposée en première intention thérapeutique pour le glioblastome. Jusqu’à maintenant, les quelques essais réalisés étaient proposés après récidive.
Inserm Oncothai Lille, CC BY
Cancer de l’amiante
Le traitement du mésothéliome (cancer de l’amiante) par PDT est également une nouveauté en France. Des études aux USA démontrent que cette technologie peut accroître la survie de 9 mois avec les traitements actuels à 51 mois. Une injection de photofrin est réalisée 24 heures avant l’intervention chirurgicale. La technique consiste, après avoir retiré la plèvre (membrane constituée par deux feuillets, un sur le poumon, l’autre sur la face interne de la paroi thoracique, à réaliser l’illumination de la cavité pleurale après remplissage d’un liquide diffusant.
La technique de la PDT intrapleurale s’est améliorée avec les années de pratique, grâce notamment à un dispositif lumineux mieux adapté permettant d’obtenir un meilleur contrôle de la dose de lumière envoyée dans la cavité au moyen de détecteur optiques miniaturisés. Cinq patients ont été traités au CHRU de Lille. Un essai de phase III, contrôlé, randomisé et multicentrique est en train de se mettre en place. Il a pour but de comparer cette nouvelle technique au traitement standard afin de déterminer son efficacité. Cet essai va nécessiter 200 patients et sera réalisé dans plusieurs hôpitaux. En fonction des résultats, il sera alors possible de faire une demande d’autorisation de mise sur le marché qui permettra la diffusion de cette nouvelle technique innovante.

Inserm Oncothai Lille, CC BY
Enfin, notre laboratoire, le LRGP avec le Laboratoire Chimie Physique Macromoléculaire de l’université de Lorraine et Oncothai ont obtenu un brevet pour développer une nouvelle molécule photoactivable sélective pour le traitement des métastases de l’ovaire. L’idée générale est la destruction des métastases microscopiques qui se développent dans tout le péritoine, par PDT, en complément d’une résection chirurgicale des métastases macroscopiques, afin de diminuer le taux de récidive des cancers ovariens.
De quoi montrer combien la recherche en PDT en France est riche et intense : nouvelles sondes, nouvelles molécules pour une meilleure pénétration de la lumière dans les tissus, développement de nanoparticules excitables non plus par la lumière mais par rayons X, photobactéricides, photodiagnostic, agents théranostiques, immunothérapie associée à la PDT, nanoparticules multifonctionnelles pour le traitement du glioblastome… La communauté française de la PDT, qui s’était réunie l’année dernière à Lille, prépare aujourd’hui l’organisation d’un congrès international qui aura lieu à Nancy du 26 au 30 octobre 2020.![]()
Céline Frochot, Directrice de recherche CNRS Laboratoire Réactions et Génie des Procédés, Université de Lorraine et Serge Mordon, Biophysicien, spécialiste des applications du laser en médecine, Institut national de la santé et de la recherche médicale (Inserm)
Cet article est republié à partir de The Conversation sous licence Creative Commons. Lire l’article original.
![]()
